Cicatrices chéloïdes : étude translationnelle des propriétés
mécaniques et fonctionnelles des fibroblastes dermiques
La qualité cicatricielle est un enjeu majeur en chirurgie plastique,
reconstructrice et esthétique et dans le traitement des brûlés. Sans
que l’on ne connaisse précisément les causes et sans que l’on puisse
le prévoir en préopératoire, certains patients présentent des
cicatrices pathologiques hypertrophiques et proliférantes que l’on
appelle cicatrices chéloïdes. Il s’agit d’un mode de cicatrisation
pathologique, suite à un traumatisme divers (plaie, acné, chirurgie,
etc.), responsable d’une cicatrice volumineuse envahissant la peau
saine adjacente. Ce type de lésion peut être très invalidant tant sur le
plan social que fonctionnel. Ce n’est pas une lésion cancéreuse, mais
une lésion bénigne liée à un processus de cicatrisation qui s’emballe
et ne parvient pas à s’arrêter. Ces cicatrices, observées plutôt
fréquemment, le sont principalement chez les peaux sombres. Ce
processus s’accompagne également de douleurs et de démangeaisons
liées qui peuvent être un véritable enfer pour la personne. Leur
mécanisme de survenue est déroutant et peut sembler aléatoire : un
patient peut présenter une cicatrice chéloïde à un endroit et aura par
ailleurs des cicatrices saines survenues dans un contexte ou dans une
localisation différente.

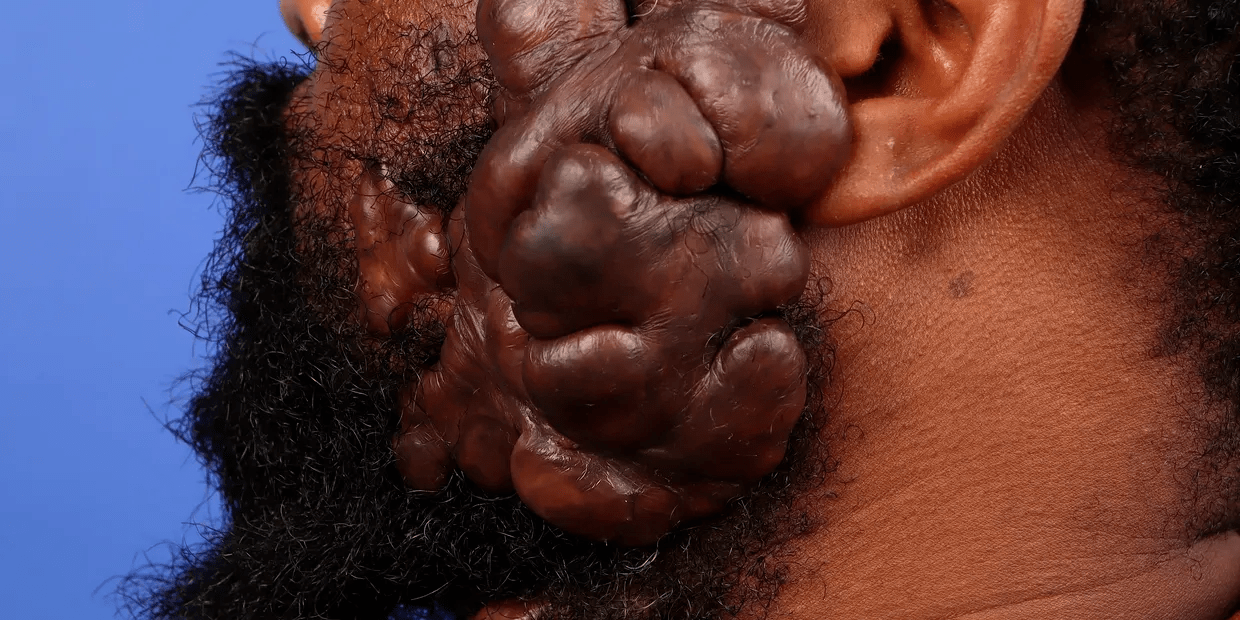
Cicatrice chéloïde
localisée sur la face,
particulièrement
invalidante sur le plan
social
Des représentations de ces cicatrices existent depuis l’Égypte ancienne, à l’époque des pyramides. Elles ont été décrites dans la littérature pour la première fois il y a un peu plus de 200 ans par Retz puis Alibert, médecin à l’Hôpital Saint-Louis à Paris. Actuellement, malgré un nombre croissant d’études scientifiques s’intéressant à ce sujet, nous ne disposons pas de véritable explication concernant le mécanisme de formation de ces cicatrices. Il serait multifactoriel (prédisposition génétique, localisation de la cicatrice sur une zone de tension cutanée, contexte de formation : brûlures plus pourvoyeuses de cicatrices chéloïdes) et il n’existe pas de traitement complètement satisfaisant. Nous disposons de plusieurs options de traitement permettant une prise en charge graduelle en fonction de la sévérité de l’atteinte. Ces traitements sont les injections intracicatricielles de corticoïdes, la radiothérapie (externe ou interne, qui n’est pas toujours envisageable selon les localisations des cicatrices et les patients, car il existe un risque de cancérisation secondaire de la zone irradiée), l’application de gels de silicone, l’injection de chimiothérapies (traitements anticancéreux responsables d’effets indésirables importants), et les traitements chirurgicaux éventuellement associés aux autres traitements mentionnés. La principale problématique de prise en charge est que les cicatrices chéloïdes ont tendance à récidiver si on les enlève, et parfois de manière plus grave.
Les études précédemment réalisées sur ces cicatrices ont permis de comprendre que l’augmentation flagrante de volume était principalement liée à une accumulation de fibres de collagène, composant normal du tissu cutané, mais dont la sécrétion est beaucoup plus abondante et mal régulée dans les cicatrices chéloïdes. Dans la peau, le fibroblaste est la cellule responsable de la production de collagène et de la matrice cutanée. Il est situé dans le derme et confère à la peau résistance, élasticité et souplesse. Dès lors, sachant que les fibroblastes sont responsables de la sécrétion excessive de collagène dans la chéloïde, il est important de mieux comprendre le fonctionnement des fibroblastes dans les cicatrices chéloïdes pour pouvoir mieux les traiter.
Un projet de recherche est actuellement développé par l’équipe du Pr Maurice MIMOUN et celle du docteur Laurence MICHEL, Chercheuse INSERM dans l’unité U976, concernant l’étude des propriétés mécaniques et fonctionnelles des fibroblastes dermiques provenant de ces cicatrices chéloïdes. Pour cette étude, nous réalisons des cultures de fibroblastes chéloïdiens à partir de chéloïdes obtenues après ablation dans le service de chirurgie et directement envoyées au laboratoire pour y être manipulées. Il s’agit alors d’analyser les caractéristiques des gènes de ces fibroblastes (par PCR quantitative ciblée de certains gènes et analyse du transcriptome entier). Le profil phénotypique des fibroblastes est étudié par la détection des protéines qu’ils expriment et qu’ils peuvent produire (Immunofluorescence et Dosage de facteurs par des techniques adaptées telles que les ELISA).
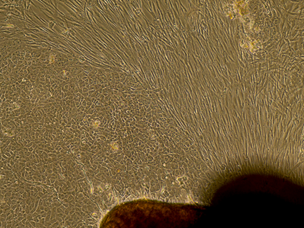
Culture de cellules qui migrent à partir d’une chéloïde opérée chez le patient vu précédemment (morceau de chéloïde visible à la partie inférieure de la photographie) : Fibroblastes de chéloïde qui sont les cellules en forme de fuseau (en haut à droite) et kératinocytes (en bas à gauche) : cellules de l’épiderme, cuboïdales, qui migrent aussi à partir des morceaux de peau.
Microscope optique, x4
Nous nous intéressons également aux fonctions des cellules et étudions leur prolifération (suivi du temps de doublement de la culture), leurs capacités de migration à l’aide d’un modèle de fermeture de plaie in vitro et leur capacité de contraction d’un gel de collagène.
Nous approfondissons davantage leurs capacités mécaniques en quantifiant les forces d’adhésion exercées par les fibroblastes chéloïdiens soumis à des contraintes données (Traction Force Microscopy). Ceci nous permet de mieux appréhender le comportement de ces fibroblastes qui semble exercer des forces de traction variables en fonction de la zone de la chéloïde et de sa localisation sur le corps humain.
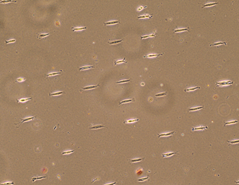
Fibroblastes de chéloïde contraints de prendre une forme rectangulaire préétablie dans des moules (« patterns ») préformés pour étudier leurs forces d’adhésion au niveau des points d’ancrage
Microscope optique, x10
Ce projet est d’autant plus innovant qu’il s’intéresse non seulement à des fibroblastes de chéloïdes localisés sur différentes zones du corps, mais aussi à différentes sous-populations de fibroblastes au sein même de la cicatrice chéloïde, à savoir au centre ou à la périphérie de la cicatrice. Nous supposons que les cellules vont avoir un comportement différent selon leur localisation centrale ou en bordure en raison des observations cliniques que nous avons réalisées chez les patients. Fréquemment, le centre des cicatrices est atrophié et contraste avec la périphérie qui est inflammatoire et plus active. Ceci n’a cependant pas été encore démontré scientifiquement et les résultats des analyses en cours devraient nous permettre de mieux comprendre les mécanismes en jeux dans le développement et l’entretien des cicatrices chéloïdes. L’objectif final est de pouvoir déduire de ces expériences, des implications thérapeutiques et améliorer ainsi la qualité de vie des patients.
Kevin Serror, Lauren Ferrero, Laurence Michel, Maurice Mimoun